ASCO热评丨李南林教授:拨云见日——HR+/HER2-早期乳腺癌辅助内分泌联合CDK4/6抑制剂强化治疗策略愈加清晰
作者:肿瘤瞭望 日期:2021/6/22 10:36:46 浏览量:9401
肿瘤瞭望版权所有,谢绝任何形式转载,侵犯版权者必予法律追究。
编者按:CDK4/6抑制剂联合内分泌治疗已经成为HR+/HER2-晚期乳腺癌的标准治疗策略。这一治疗策略也在尝试向辅助强化阶段进行探索,其中在2020年SABCS中报道的monarchE达到主要研究终点,引起关于内分泌辅助强化治疗策略的热议。在刚刚落幕的2021年ASCO会议中报道了monarchE研究中接受新辅助化疗患者亚组的疗效和安全性(Abs 517),这一报道令内分泌联合CDK4/6抑制剂辅助强化策略愈加清晰,肿瘤瞭望特邀请到空军军医大学西京医院李南林教授对该项研究结果进行解读。
研究简介
monarchE是一项开放、随机、全球多中心3期临床研究,旨在评估Abemaciclib(2年治疗)联合内分泌(ET)对比单用ET治疗HR+/HER2-的高危早期乳腺癌的疗效和安全性。研究中高危的定义为:≥4 枚阳性腋窝淋巴结(ALN)或1~3枚阳性ALN以及至少符合以下情况之一:肿瘤≥5 cm;组织学分级3级;中心实验室检测的Ki-67≥20% 。随访19.1个月(2020SABCS Abs GS1-01), 达到主要研究终点IDFS, P=0.0009,HR(95%CI): 0.713(0.583,0.871)。2年的IDFS率在Abemaciclib+ET组为92.3%,在单用ET组为89.3%,绝对值差异为3.0%。关键次要研究终点DRFS,P=0.0009, HR(95%CI): 0.687(0.551,0.858)。2年的DRFS率在Abemaciclib+ET组为93.8%,在单用ET组为90.8%,绝对值差异为3.0%。这一阳性结果的报道给高危早期乳腺癌辅助内分泌联合Abemaciclib强化治疗策略奠定了坚实的依据,具有非常广阔的应用前景。2021年ASCO中报道了monarchE中501例中国人群的疗效(Abs 522),结果显示与全球人群一致,为未来在中国人群的应用提供了相应证据。对于预期复发风险较高患者(如肿瘤体积大、淋巴结转移阳性)术前会选择进行新辅助化疗(NAC),但NAC达到病理学缓解(pCR)通常有限(<10%),提示这一类人群需要辅助内分泌强化治疗。2021年ASCO报道其中2056例患者接受过NAC人群(占monarchE研究IIT人群的36%)的疗效和安全性(Abs 517)。大多数患者接受了标准NAC治疗(蒽环类药物联合紫杉烷),两组之间平衡。接受NAC的患者在初诊时肿瘤体积更大,更常见于绝经前患者(约50%)。虽然是事后分析,但样本量达2000例以上对于新辅助/辅助治疗的研究难能可贵,且接受NAC种类以及基线特征与实际临床情况相似,非常具有指导意义,值得高度关注。



IDFS结果显示P=0.0002,HR(95%CI):0.614(0.473,0.797),其中HR比ITT人群更小。Abemaciclib+ ET组的2年IDFS率为87.2%,单用ET组为80.6%,绝对值差异为 6.6%,比ITT人群的3%更大。DRFS结果显示P=0.0006,HR(95%CI):0.609(0.459,0.809),其中HR比ITT人群更小。Abemaciclib+ ET组的2年DRFS率为89.5%,ET组为82.8%,绝对值差异为6.7%,比ITT人群的3%更大。绝对值差异达6%以上可以说是一个很大的突破,提示在接受NAC的患者中,Abemaciclib+ ET在IDFS和DRFS方面可能较ITT人群具有更优的临床意义的治疗获益。
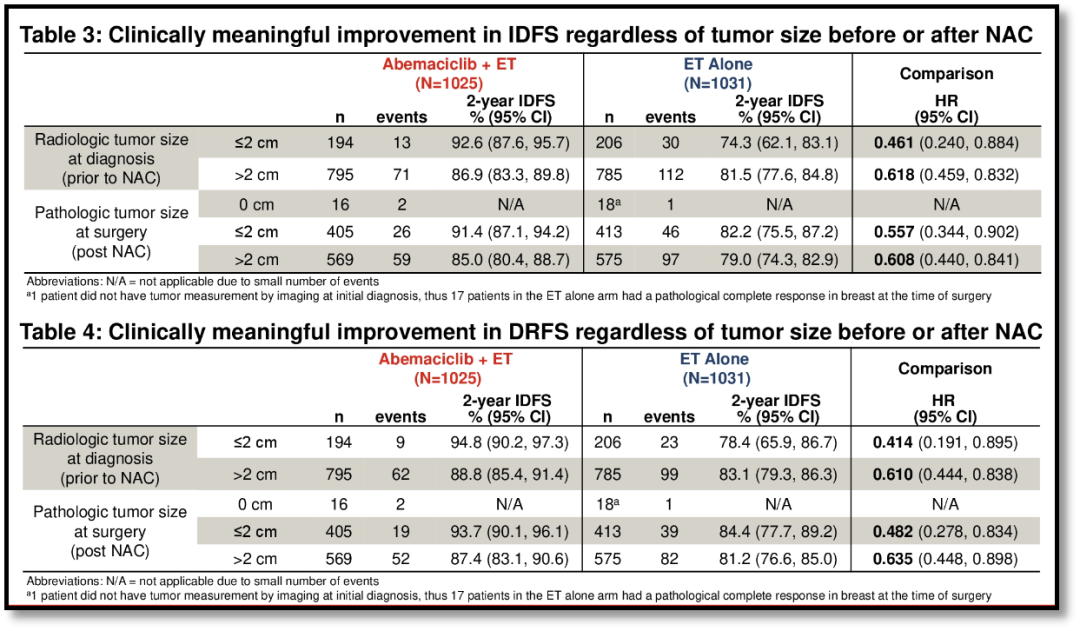
进一步分析显示无论NAC前后的肿瘤大小(以2cm为界值),IDFS和DRFS均出现具有临床意义的改善,提示与NAC前后的肿瘤大小无关(≤2 cm vs >2 cm),Abemaciclib+ET均降低了既往接受NAC患者发生IDFS事件或DRFS事件的风险。

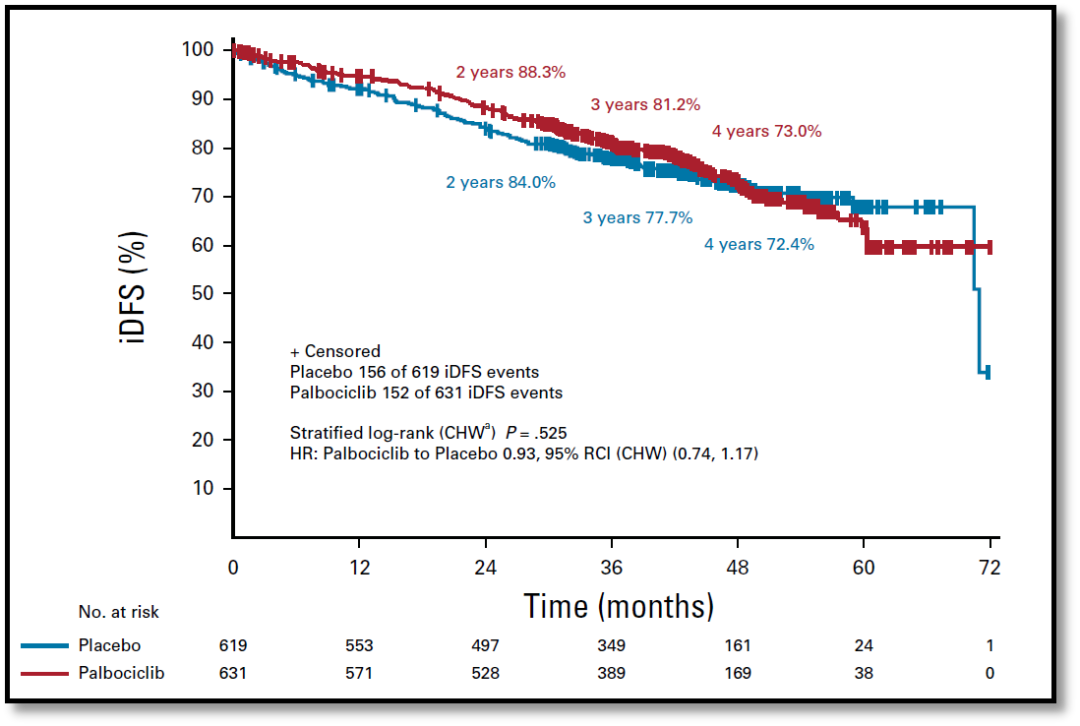
安全性数据与总体安全性人群相似,其中最常见的不良事件是腹泻(联合组:任何级别82.5%,3级8.2%,4级0%,5级0.1%),与阿贝西利的已知特征一致。PENELOPE-B是一项接受NAC治疗后的辅助ET联合Palbociclib的3期研究(J Clin Oncol, 2021, 39:1518-1530.)。该研究纳入HR+HER2-早期乳腺癌完成NAC后行手术治疗non-pCR且CPS-EG评分≥3或2且ypN+患者。入组后接受Palbociclib(1年治疗)+ET或ET,主要研究终点为iDFS。随访42.8个月,结果显示未达到主要研究终点,P=0.525,HR(95%RCI):0.93(0.74,1.17)。2年的iDFS率在Abemaciclib+ET组为88.3%,在单用ET组为84%,绝对值差异为4.3%,低于monarchE研究中接受NAC亚组2年IDFS率绝对差异6.6%,提示Abemaciclib在这一高危人群中有更好的获益可能,但仍需要进一步随机对照研究验证。
选择的药物不同:a.Abemaciclib和Palbociclib都是选择性CDK4和CDK6激酶的活性抑制剂。但对CDK4和CDK6抑制的差异可能导致药物在不同组织中产生不同的效应。CDK4参与乳腺以及乳腺肿瘤形成,CDK6与造血干细胞周期有一定相关性。Abemaciclib对CDK4的高度选择性,是CDK6的(近)14倍(Oncotarget. 2017;8(41)69493-69507.)。b.Abemaciclib为连续服用,Palbociclib为用3周停1周,是否不同的用药方式会对生存结局有一定影响,还需要更多的研究给以答案;c.Abemacicilb和Palbociclib在晚期乳腺癌的内分泌联合治疗HR+HER2-乳腺癌3期临床研究均显示相对于单用内分泌显著延长PFS,但联合氟维司群的3期研究MONARCH 2和PALOMA 3的OS结果却相左;d.Abemaciclib辅助内分泌强化治疗的Monarch E研究取得阳性结果,而Palbociclib的PALLAS以及PENELOPE-B结果均为阴性;e.安全谱不同,Abemaciclib不良反应以腹泻为主,Palbociclib以中性粒细胞减少为主。以上均提示Abemaciclib和Palbociclib虽然同为CDK4/6抑制剂,在作用机制、疗效及安全性方面还是有一定差异的。用药时长不同:monarchE研究中Abemaciclib用药时长为2年,PENELOPE-B研究为Palbociclib用药时长1年。是否2年的辅助内分泌加强为更好的时长选择,也等待更多的研究来回答,其中包括Ribociclib的NATALEE研究也会给我们更多的启示。人群的选择:PENELOPE-B研究为入组NAC后non-pCR患者,monarchE研究亚组分析则将接受NAC患者均纳入分析,提示其中可能包含pCR的患者,依据既往NAC的pCR率通常<10%,这一部分人群比例并不高。因此,这方面人群差异可能并不大。但monarchE研究总体设计入组筛选时依据ALN和Ki-67进行选择,提示ALN和Ki-67有可能对高危人群的筛选更为精准。综合以上,2021ASCO发布的monarchE研究接受NAC亚组人群疗效和安全性的数据令我们对于CDK4/6抑制剂联合内分泌治疗策略在药物选择、时长以及人群筛选等等方面都有进一步清晰的了解认识,同时也期待更长的随访数据以及更多的研究报道让CDK4/6抑制剂真正可以造福更广大乳腺癌患者。
空军军医大学西京医院甲状腺乳腺血管外科
医学博士,副主任医师,副教授,硕士生导师
中国抗癌协会乳腺癌专业委员会委员
中国临床肿瘤学会(CSCO)乳腺癌专家委员会委员
中国临床肿瘤学会(CSCO)患者教育专家委员会委员
陕西省抗癌协会乳腺癌专业委员会常委、秘书
陕西省抗癌协会抗癌药物专业委员会常委
陕西省抗癌协会肿瘤综合治疗专业委员会委员
本内容仅供医学专业人士参考
相关搜索
乳腺癌





 京公网安备 11010502033352号
京公网安备 11010502033352号