CDK4/6抑制剂作为一种特异性细胞周期靶向药物,在临床前的转化研究中展现出强大的抑癌效果,并且在临床试验阶段表现卓越,PALOMA、MONARCH、MONALEESA系列研究数据不断推陈出新,开启了HR阳性晚期乳腺癌的CDK4/6抑制剂时代。过去一年中,CDK4/6抑制剂携多项试验的OS数据重磅亮相,在内分泌敏感及耐药领域各领风骚;值此春暖花开之际,我们就CDK4/6抑制剂在HR阳性晚期乳腺癌年度研究进展做如下梳理。
1、内分泌敏感人群——旗开得胜,硕果累累
MONALEESA-7研究 OS数据 (2019 ASCO)
作为CDK4/6抑制剂唯一的一项仅用于绝经前/围绝经期HR阳性晚期乳腺癌一线内分泌治疗的临床试验,MONALEESA-7研究,在2019年ASCO大会上,携总生存(OS)显著获益的优秀数据重磅亮相。MONALEESA-7研究共纳入672例绝经前/围绝经期HR阳性HER2阴性晚期乳腺癌患者,要求既往晚期未接受内分泌治疗(endocrine therapy,ET),允许不超过一线的晚期化疗,1:1随机分为Ribociclib+他莫昔芬/NASI+戈舍瑞林组(N=335)和安慰剂+他莫昔芬/NASI+戈舍瑞林组(N=337)。从入组人群特征来看,约60%的人群为初诊IV期或者既往未接受(新)辅助内分泌治疗,约40%既往曾接受(新)辅助内分泌治疗,这其中约10%为完成辅助内分泌治疗12个月以后出现疾病复发,约30%为完成辅助内分泌治疗12个月以内复发,值得注意的是,基于目前内分泌耐药性的判定,这30%的人群应归类于继发性内分泌耐药或者早期复发,但这部分人群在(新)辅助内分泌治疗阶段并未使用过卵巢功能抑制联合AI类药物,换句话说,MONALEESA-7研究所纳入的人群均无AI类药物治疗史,理论上这些人群属于内分泌敏感人群(或称之为AI敏感人群)。
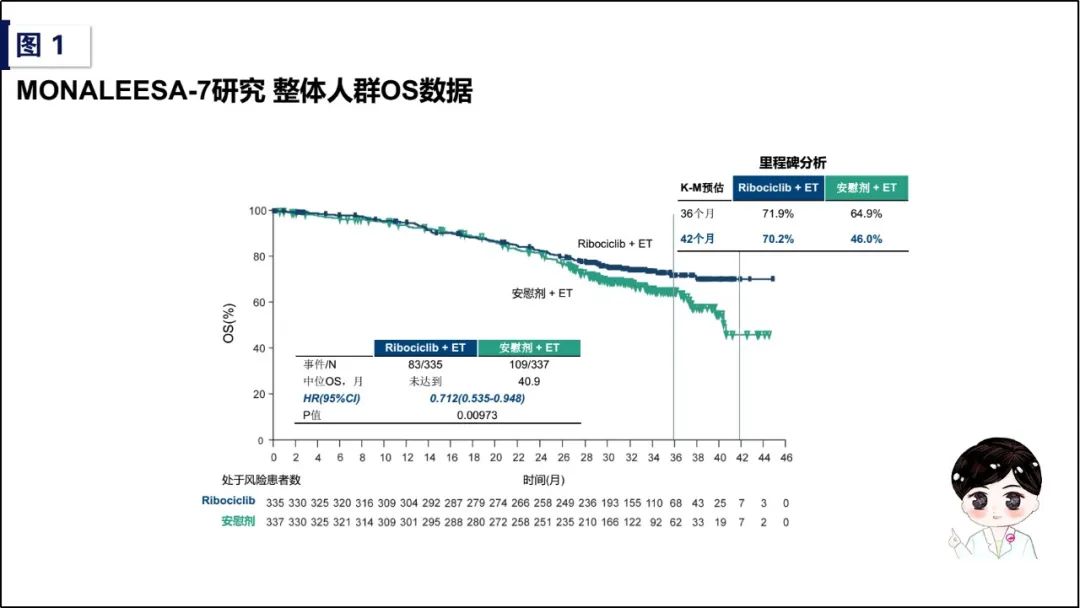
2018年公布的初始分析结果显示整体人群的主要研究终点PFS,Ribociclib + ET为23.8个月,对照组安慰剂+ET为13.0个月(HR值为0.55 [95%CI,0.44-0.69];P<0.0001)。此次2019年ASCO大会所公布的OS结果为次要研究终点,从整体人群来看,对照组安慰剂 + ET的中位OS为40.9个月,Ribociclib + ET中位OS尚未达到(NR,HR值为0.712 [95%CI,0.535-0.948],P=0.00973),差别具有显著统计学意义;从预设内分泌联合药物NSAI亚组来看,对照组安慰剂+ET(247/347)的中位OS为40.9个月,Ribociclib + ET(248/335)中位OS尚未达到(NR,HR值为0.699 [95%CI,0.501-0.976]),与整体人群OS结果相一致,同时也验证了我们上述对这部分人群内分泌敏感性的推断。综上,MONALEESA-7研究首次在HR阳性HER2阴性晚期乳腺癌患者中观察到CDK4/6抑制剂联合ET能够显著改善OS,拉开了2019年CDK4/6抑制剂在HR阳性晚期乳腺癌的年度盛典帷幕!

MONALEESA-3研究 一线人群OS数据 (2019 ESMO)
无独有偶,MONALEESA-3研究基于其巧妙的研究设计,让我们得以在2019年领略到CDK4/6抑制剂在绝经后内分泌敏感人群一线治疗的总生存获益情况。MONALEESA-3研究共纳入726例绝经后女性和男性HR阳性HER2阴性晚期乳腺癌患者,允许既往接受过≤1线内分泌治疗,2:1随机分为Ribociclib+氟维司群(N=484)和安慰剂+氟维司群组(N=242)。从入组人群特征来看,MONALEESA-3研究纳入了367例treatment naïve的人群(试验组238例,对照组129例),包括初诊IV期尚未接受内分泌治疗、或完成辅助内分泌治疗12个月以后出现疾病复发尚未接受内分泌治疗,理论上这些人群属于内分泌敏感的一线人群。
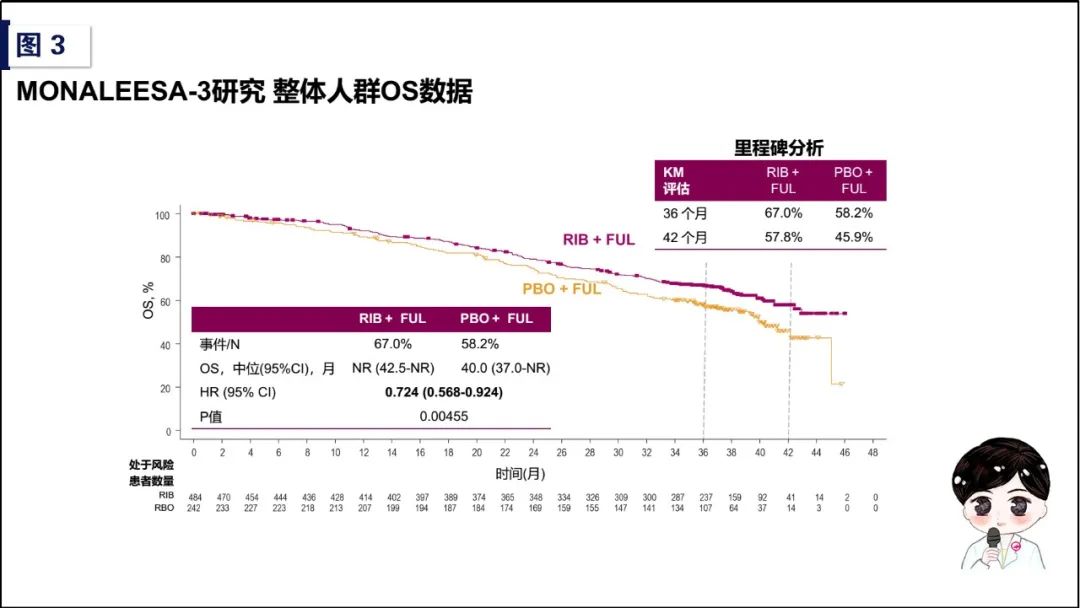
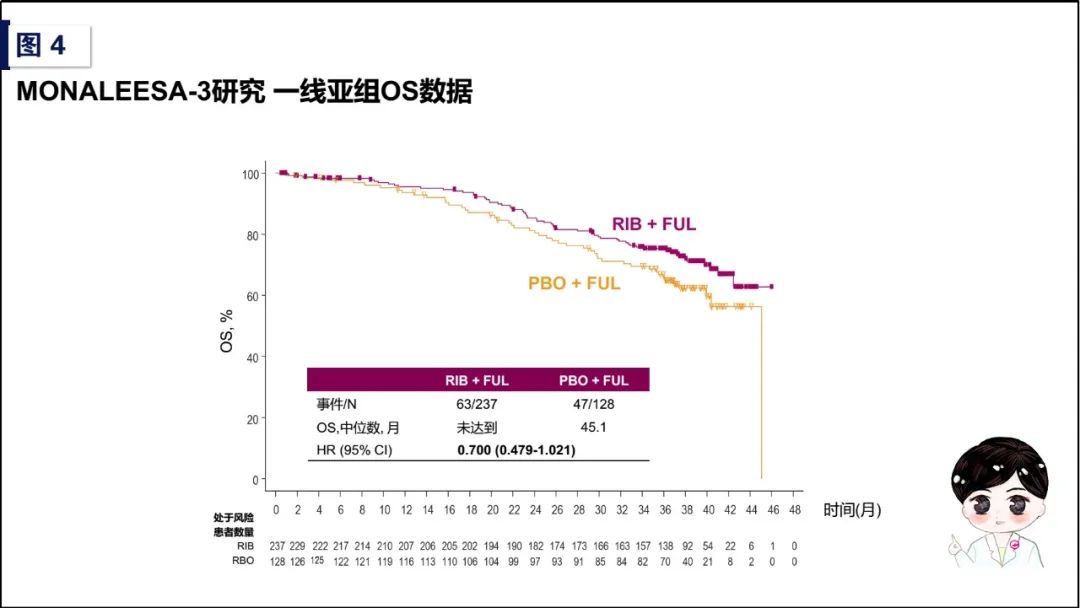
同样是2018年公布的初始分析结果显示,整体人群的主要研究终点PFS,Ribociclib +氟维司群为20.6个月,对照组安慰剂+氟维司群为12.8个月(HR值为0.587 [95%CI,0.488-0.705]);对于内分泌敏感的一线治疗亚组,Ribociclib +氟维司群作为一线治疗,使中位PFS时间由对照组的19.2个月提高到33.6个月(HR值为0.546 [95%CI,0.415-0.718])。2019年ESMO大会公布的OS结果为次要研究终点,从整体人群来看,对照组安慰剂+氟维司群的中位OS为40.0个月,Ribociclib +氟维司群中位OS尚未达到(NR,HR值为0.724 [95%CI,0.568-0.924],P=0.00455),差别具有显著统计学意义;对于内分泌敏感的一线治疗亚组,对照组的中位OS为45.1个月,试验组的中位OS尚未达到(NR,HR值为0.700[95%CI,0.479-1.021],尽管并无显著统计学差异,但基于Ribociclib +氟维司群组的一线人群尚未达到中位OS,我们有信心期待最终的随访结果能够再次印证CDK4/6抑制剂在HR阳性晚期乳腺癌中的盛世花开!
2、内分泌耐药人群——山重水复,柳暗花明
MONALEESA-3研究 早复发+二线人群OS数据 (2019 ESMO)
CDK4/6抑制剂在内分泌敏感人群一线治疗领域攻城略池的骄人战绩,让我们对其在克服内分泌耐药领域有了更多的盼望和期待。尽管PALOMA-3研究的OS数据让我们看到了CDK4/6抑制剂攻克内分泌耐药的曙光(试验组Pabociclib +氟维司群的中位OS为34.9个月,对照组安慰剂+氟维司群的中位OS为28.0个月),但这6.9个月的OS获益并未达到预设统计学差异(HR值为0.814 [95%CI,0.644-1.029]),这主要是由于PALOMA-3研究纳入了晚期多线内分泌治疗、并且不超过晚期一线化疗的患者,如此繁杂的入组人群特征反而让我们期待CDK4/6抑制剂能够在更加“纯粹”的内分泌耐药背景下带来新的惊喜。
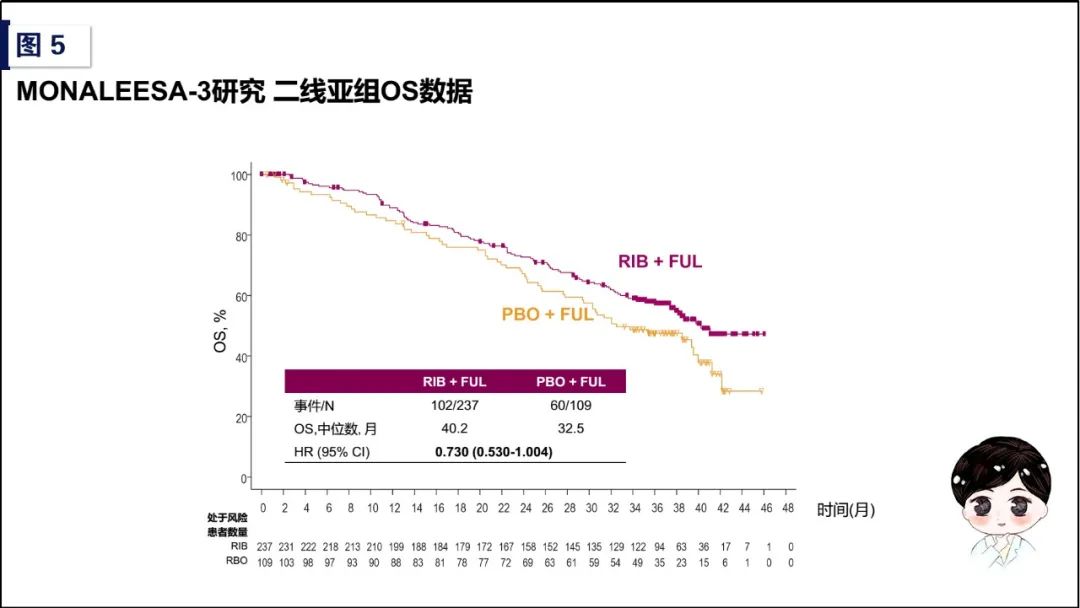
怀揣着上述期待,2019年ESMO大会同时公布的MONALEESA-3研究和MONARCH-2研究OS数据交出了令人满意的答卷。两项研究的入组条件更加严格,要求二线人群仅且接受过晚期一线内分泌治疗,且不允许接受晚期化疗。MONALEESA-3研究如前所述,其巧妙之处在于不仅纳入了treatment naïve的人群,还纳入了345例二线人群(试验组236例,对照组109例),包括辅助内分泌治疗中或完成辅助内分泌治疗12个月以内复发、以及初诊IV期和完成辅助内分泌治疗12个月以后复发一线内分泌治疗进展的患者。2018年公布的初始分析结果已经显示,Ribociclib +氟维司群能够使这部分内分泌耐药亚组的中位PFS时间由对照组的9.1个月提高到14.6个月(HR值为0.571 [95%CI,0.443-0.737])。此次公布的OS数据,在整体人群OS结果显著获益的前提下,对于这部分内分泌耐药的二线治疗亚组,对照组安慰剂+氟维司群的中位OS为32.5个月,试验组Ribociclib +氟维司群的中位OS为40.2个月(HR值为0.730[95%CI,0.530-1.004],7.7个月的绝对获益,对于OS作为次要研究终点的亚组分析已属不易,并且使得PFS的良好趋势(绝对获益5.5个月)在后续治疗过程中得以保持,结果同样让我们感到欣喜。
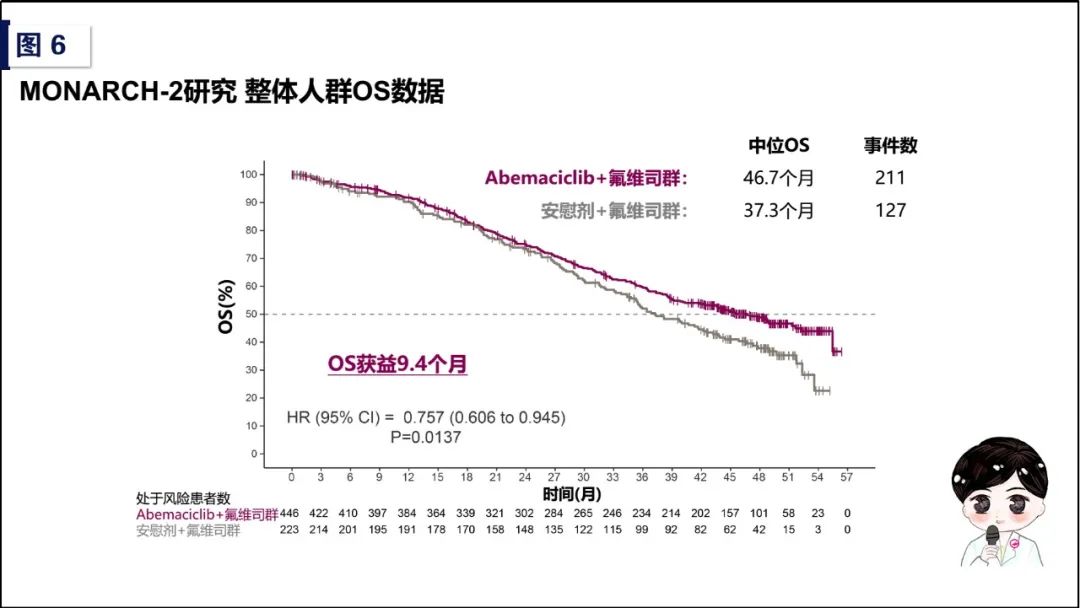
MONARCH-2研究 OS数据 (2019 ESMO)
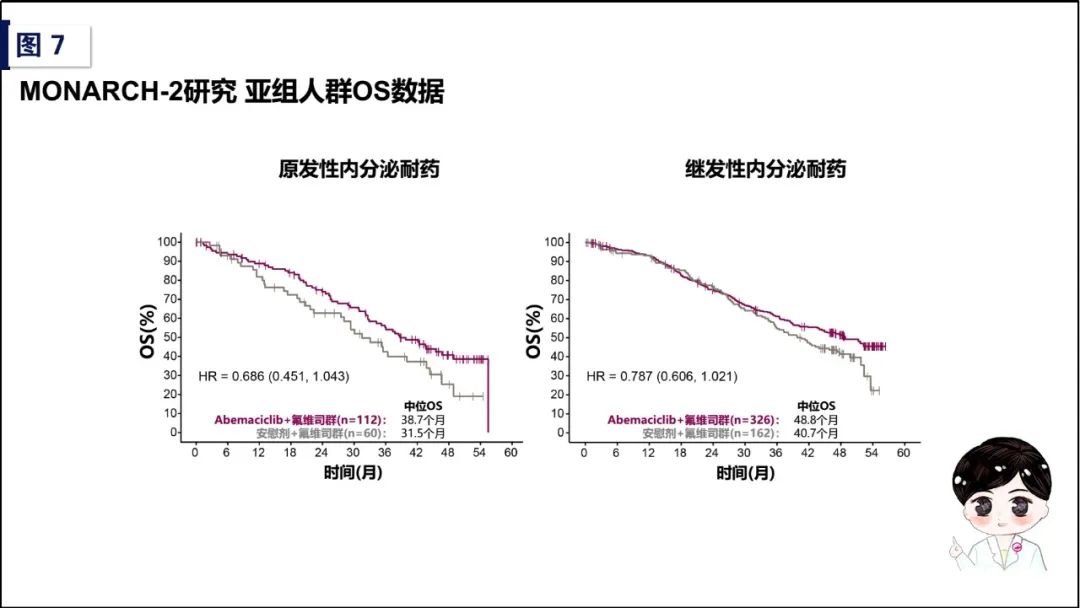
最让我们感到振奋的,当属MONARCH-2研究于2019年ESMO大会所公布的OS数据。相比PALOMA-3研究和MONALEESA-3研究,MONARCH-2研究对于耐药人群的选择和耐药性的界定最为苛刻,共纳入669例绝经前/围绝经期或绝经后HR阳性HER2阴性晚期乳腺癌患者,包括25.7%的原发性内分泌人群和74.3%的继发性内分泌耐药人群,2:1随机分为Abemaciclib+氟维司群(N=446)和安慰剂+氟维司群组(N=223)。此次ESMO大会公布的最新数据,在主要研究终点PFS持续获益的前提下(试验组 vs 对照组:16.9个月 vs 9.3个月,HR值为0.536 [95%CI,0.445-0.645];P<0.0001),OS作为次要研究终点,在整体人群中达到了显著性差异:试验组Abemaciclib+氟维司群为46.7个月,对照组安慰剂+氟维司群为37.3个月(HR值为0.757 [95%CI,0.606-0.945];P=0.0137)。尽管基于内分泌耐药性的分层分析,原发性及继发性内分泌耐药亚组的OS数据未达显著统计学差异(原发性耐药亚组,试验组 vs 对照组:38.7个月vs 31.5个月,HR值为0.686[95%CI:0.451-1.043];继发性耐药亚组,试验组 vs 对照组:48.4个月vs 40.7个月,HR值为0.787[95%CI:0.606-1.021]),但总体来看瑕不掩瑜,MONARCH-2研究的OS数据与PFS数据交相辉映,让我们在内分泌耐药领域山重水复的探索中,第一次切切实实地领略到了CDK4/6抑制剂带来的柳暗花明!
3、中国人群——不忘初心,笃定前行
MONARCH plus研究(2019 ESMO)
随着CDK4/6抑制剂临床试验如火如荼、全线开花的进行,我们必须要冷静的思考:无论是一线探索的PALOMA-2、MONARCH-3、MONALEESA-2、MONALEESA-7研究,还是二线探索的PALOMA-3、MONARCH-2、MONALEESA-3研究,所纳入的中国患者群体数量均是非常有限的,即便是可以根据地域来进行分层分析,但这种小样本量的探索性亚组分析很难改变临床实践。那么这些铺天盖地的喜人数据,对于我们中国乳腺癌患者群体的临床指导意义究竟有多大?幸运的是,由江泽飞教授牵头发起的、我们中心有幸参与的MONARCH plus研究,让我们在乱花渐欲迷人眼的困扰中看到了前行的出路和方向。
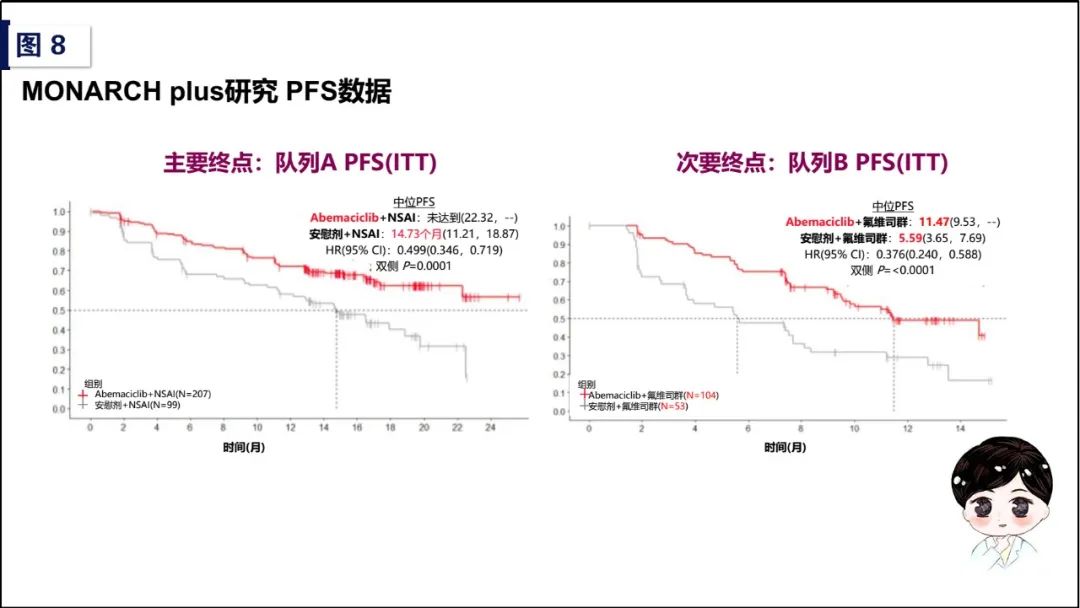
MONARCH plus研究共纳入463例绝经后HR阳性HER2阴性晚期乳腺癌患者,分为两个队列:队列A(N=306)纳入的是既往没有接受过系统性治疗的转移或局部复发性疾病、或完成辅助内分泌治疗>1年或没有接受辅助内分泌治疗后复发、或完成辅助内分泌治疗小于1年或正在接受辅助内分泌治疗(来曲唑或阿那曲唑除外)复发、或首诊4期没有接受过内分泌治疗,2:1随机分为Abemaciclib+NSAIs和安慰剂+NSAIs;队列B(N=157)纳入的是辅助来曲唑或阿那曲唑治疗治疗期间或1年内复发(进展后未再接受内分泌治疗)、或从辅助内分泌治疗完成后> 1年且在接受一线内分泌治疗之后复发、或首诊IV期且一线内分泌治疗后复发,要求转移性疾病不超过1线内分泌治疗且没有接受晚期化疗,2:1随机分为Abemaciclib+氟维司群和安慰剂+氟维司群。2019年ESMO大会所公布的是主要终点:队列A的PFS,和关键次要终点:队列B的PFS,从结果来看,队列A,也就是内分泌敏感人群(或者称之为AI敏感人群)的PFS,试验组 vs 对照组:未达到 vs 14.73个月,HR值为0.499 [95%CI,0.346-0.719],P=0.0001,具有显著统计学差异,与一线治疗的MONARCH-3研究PFS数据基本一致(试验组 vs 对照组:未达到 vs 14.7个月,HR值为0.54 [95%CI,0.41-0.72],P=0.000021);队列B(或称之为内分泌耐药人群)的PFS,试验组 vs 对照组:11.47个月 vs 5.59个月,HR值为0.376 [95%CI,0.240-0.588],P≤0.0001,同样具有显著统计学差异,与二线治疗的MONARCH-2研究PFS获益趋势相同(试验组 vs 对照组:16.4 vs 9.3个月,HR值为0.553 [95%CI,0.499-0.681],P<0.0000001)。MONARCH plus研究的PFS数据,让我们能够不忘初心,在2019年不断刷新的CDK4/6抑制剂数据浪潮中,为中国HR阳性乳腺癌患者做出坚定的抉择!
4、三阳性晚期乳腺癌人群——另辟蹊径,崭露头角
MonarcHER研究(2019 ESMO)
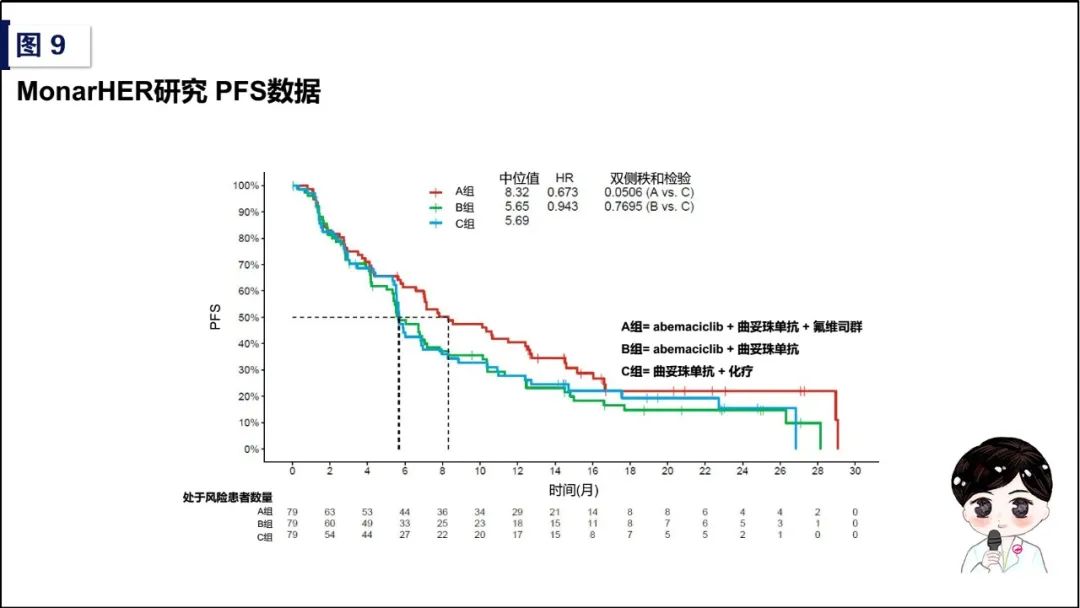
如果说CDK4/6抑制剂联合内分泌治疗的OS数据是2019年度的重磅亮相,那么本年度的另一出精彩乐章便是MonarcHER研究。作为首个在HR阳性HER2阳性晚期乳腺癌领域探索CDK4/6抑制剂+内分泌治疗+抗HER2治疗的II期临床试验,MonarcHER研究纳入了237例HR阳性HER2阳性晚期乳腺癌患者,要求在晚期阶段接受过≥2次抗HER2治疗并且接受过T-DM1和紫杉醇治疗、未接受过CDK4/6抑制剂或氟维司群治疗,1:1:1随机分为A组:Abemaciclib+氟维司群+曲妥珠单抗、B组:Abemaciclib+曲妥珠单抗、C组:曲妥珠单抗+研究者所选择化疗方案。2019年ESMO大会公布的PFS数据显示,A组vs C组:8.32个月vs 5.69个月,HR值为0.673,双侧秩和检验为0.0505(预先设定双侧α检验为0.2),具有显著统计学差异;B组vs C组未观察到PFS获益,提示内分泌手段的联合不可或缺。虽然PFS绝对获益仅为2.63个月,但这对于多线抗HER2治疗进展的晚期乳腺癌患者来说已属不易,CDK4/6抑制剂联合内分泌的加入,为2线及以上抗HER2治疗进展的三阳型MBC,提供了新的出路和方向,在三阳性晚期乳腺癌初露锋芒!
综上,基于 CDK4/6抑制剂的不同临床试验让我们看到其在内分泌敏感的HR阳性HER2阴性晚期乳腺癌一线治疗的霸主地位;在内分泌耐药的人群中初露端倪,仍然需要大型随机对照的临床试验证实,能否雄踞二线仍需谨慎;在中国HR阳性HER2阴性乳腺癌群体中获得与国际多中心临床试验异曲同工的效果,为中国晚期乳腺癌患者应用CDK4/6抑制剂添上浓墨重彩的一笔;在三阳性晚期乳腺癌患者中勇于尝试,结果值得期待,淋漓尽致地展现了CDK4/6抑制剂开疆拓土的决心;总之,2019年CDK4/6抑制剂在HR阳性晚期乳腺癌研究领域星光熠熠,期待2020年更加精彩纷呈!
[1] Im S, Lu Y, Bardia A, et al. Overall Survival with Ribociclib plus Endocrine Therapy in Breast Cancer. N Engl J Med. 2019; 381(4): 307-316.[2] Slamon D, Neven P, Chia S, et al. Overall Survival with Ribociclib plus Fulvestrant in Advanced Breast Cancer. N Engl J Med. 2020; 382(6): 514-524[3]George W. Sledge J, Masakazu T, et al. MONARCH-2: Overall survival of abemaciclib plus fulvestrant in patients with HR+, HER2- advanced breast cancer. 2019 ESMO[4]Z. jiang, X. Hu, Q, Zhang, et al. MONARCH plus: A phase 3 trial of abemaciclib plus nonsteroidal aromatase inhibitors (NSAIs) or fulvestrant (FULV) for women with HR+/HER2- advanced breast cancer(ABC). 2019 ESMO[5] Sara M, Andrew M , Stefania Z, et al. monarcHER: A randomized phase 2 study of abemaciclib plus trastuzumab with or without fulvestrant versus trastuzumab plus standard of care chemotherapy in women with HR+, HER2+ advanced breast cancer (ABC). 2019 ESMO
医学博士,教授,博士研究生导师
大连医科大学附属二院乳腺肿瘤内科主任
辽宁省百千万人才百人层次
中国肿瘤临床学会理事
中国抗癌协会乳腺癌专业委员会委员
中国临床肿瘤学会乳腺癌专家委员会委员
辽宁省医学会肿瘤分会副主任委员
辽宁省抗癌协会癌症与姑息康复医学会候任主委
中国医药教育协会乳腺疾病专业委员会沈阳学组副主任委员
中国研究型医院学会精准医学与MDT专业委员会乳腺学组副组长
大连医科大学附属第二医院肿瘤内科 主治医师
主持国家自然科学基金青年基金项目1项、辽宁省自然科学基金面上项目1项、辽宁省博士科研启动基金项目1项、大连市科技创新基金项目1项,以第一作者及通讯作者发表SCI论文6篇,累积影响因子30分
获评2019年辽宁省百千万人才工程“万”人层次,担任“中华医学会肿瘤学分会乳腺肿瘤学组青年委员会委员”、“中国抗癌协会整合肿瘤学分会青年委员会委员”等学术任职
荣获2018年临床研究进展”中国最具潜力青年肿瘤医生10强、2019年“泰然而立·话沙聚贤”乳腺病例赛全国总决赛冠军、2019年CSCO·三生肿瘤CIT中青年医师辩论赛全国总决赛冠军及最佳辩手、2019年CSCO“35 under 35”最具潜力青年肿瘤医师35强、2019年CBCS乳腺肿瘤菁英赛全国总决赛冠军
?





 京公网安备 11010502033352号
京公网安备 11010502033352号